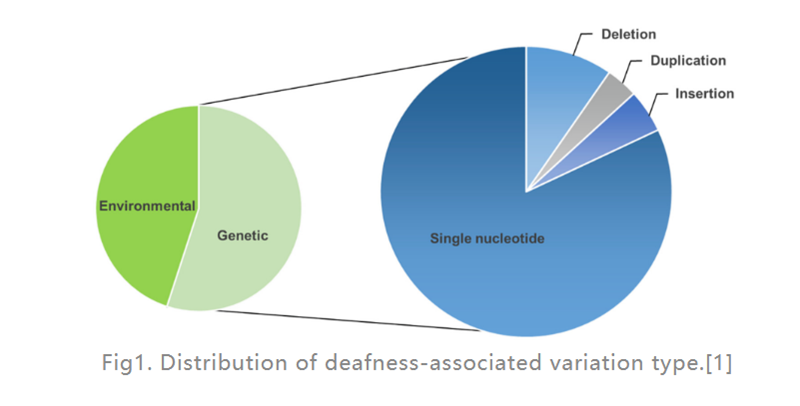
Губењето на слухот (HL) е најчеста болест со сензорна попреченост кај луѓето.Во развиените земји, околу 80% од случаите на предјазична глувост кај децата се предизвикани од генетски фактори.Најчести се дефектите на еден ген (како што е прикажано на слика 1), откриено е дека 124 генски мутации се поврзани со несиндромско губење на слухот кај луѓето, а останатите се предизвикани од фактори на животната средина.Кохлеарен имплант (електронски уред поставен во внатрешното уво кој обезбедува електрична стимулација директно на аудитивниот нерв) е убедливо најефективната опција за лекување на тешка ХЛ, додека слушно помагало (надворешен електронски уред кој ги конвертира и засилува звучните бранови) може да им помогне на пациентите со умерена ХЛ.Сепак, во моментов нема достапни лекови за лекување на наследниот HL (GHL).Во последниве години, генската терапија добива сè поголемо внимание како ветувачки пристап за лекување на дисфункција на внатрешното уво.
Сл1.Дистрибуција на типот на варијација поврзана со глувоста.[1]
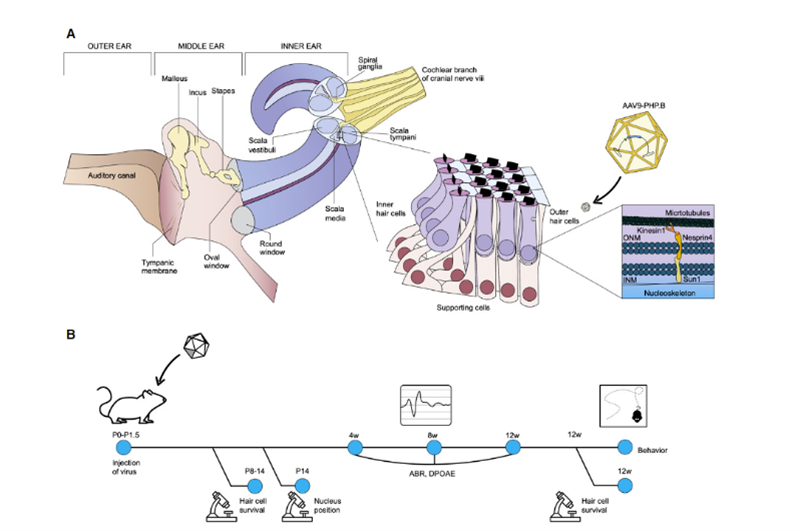
Неодамна, научниците од Институтот Салк и Универзитетот во Шефилд објавија резултат од истражувањето во Молекуларна терапија - методи и клинички развој [2], кој покажа широки изгледи за примена за in vivo генска терапија на наследна глувост.Ури Манор, асистент-професор за истражување на Институтот Салк и директор на Центарот за напредна биофотоника Вејт, рече дека е роден со тешко губење на слухот и смета дека враќањето на слухот би било прекрасен подарок.Неговите претходни истражувања открија дека Eps8 е регулаторен протеин на актин со активности за врзување и покривање на актин;во клетките на кохлеарната коса, протеинскиот комплекс формиран од Eps8 со MYO15A, WHIRLIN, GPSM2 и GNAI3 главно постои.Затоа, Eps8 може да ја регулира должината на стереоцилијата на влакното, што е од суштинско значење за нормална функција на слухот;Бришењето или мутацијата на Eps8 ќе доведе до кратка стереоцилија, што го прави неспособен правилно да го конвертира звукот во електрични сигнали за перцепција на мозокот, што пак води до глувост..Во исто време, соработникот Валтер Маркоти, професор на Универзитетот во Шефилд, откри дека клетките на косата не можат нормално да се развиваат во отсуство на Eps8.Во оваа студија, Манор и Маркоти се здружија за да истражат дали додавањето Eps8 на стереоцилијарните клетки може да ја врати нивната функција и, пак, да го подобри слухот кај глувците.Истражувачкиот тим го користеше векторот на адено-асоцираниот вирус (AAV) Anc80L65 за да ја испорача секвенцата за кодирање која содржи EPS8 од див тип во кохлеата на Eps8-/- новородените P1-P2 глувци со вбризгување на мембрана со кружен прозорец;во клетките на кохлеарната коса на глувчето Функцијата на стереоцилија беше поправена пред да созреат;а ефектот на поправка се карактеризира со технологија на слика и мерење на стереоцилија.Резултатите покажаа дека Eps8 ја зголемил должината на стереоцилијата и ја вратил функцијата на влакното во клетките со ниска фреквенција.Тие, исто така, откриле дека со текот на времето, клетките се чини дека ја губат својата способност да бидат спасени со оваа генска терапија.Импликацијата е дека овој третман можеби ќе треба да се администрира во матката, бидејќи Eps8-/- влакнестите клетки можеби созреале или акумулирале оштетување кое не може да се поправи по раѓањето на глувците.„Eps8 е протеин со многу различни функции и има уште многу да се истражи“, рече Манор.Идните истражувања ќе вклучуваат истражување на ефектот на генската терапија Eps8 во обновувањето на слухот во различни развојни фази и дали е можно да се продолжат можностите за лекување.Случајно, во ноември 2020 година, професорот KarenB Avraham од Универзитетот во Тел Авив во Израел ги објави своите резултати во списанието EMBO Molecular Medicine [3], користејќи иновативна технологија за генска терапија за да создаде безопасен синтетички адено-асоциран вирус AAV9-PHP.Б, Дефектот на генот во клетките на косата кај глувците Syne4-/- беше поправен со инјектирање на вирус кој ја носи кодираната секвенца на Syne4 во внатрешното уво на глувците, дозволувајќи му да влезе во клетките на косата и да го ослободи пренесениот генетски материјал, овозможувајќи им да созреат и нормално да функционираат (како на слика 2).
Сл.2.Шематски приказ на анатомијата на внатрешното уво, со фокус на органот на Корти и клеточната функција на несприн-4.
Може да се види дека употребата на генска терапија за постигнување на целта за лекување на наследни болести на генско ниво со вметнување, отстранување или корекција на било какви мутирани гени за лекување (односно контролирање на генетските промени во болеста) има висок клинички ефект.изгледите за апликација.Тековните методи на генска терапија за генетски дефицитарната глувост може да се поделат во следниве категории:
замена на ген
Замената на генот е веројатно „најдиректната“ форма на генска терапија, базирана на идентификување и замена на дефектен ген со нормална или див тип на копија на генот.Прва успешна студија за генетска терапија на внатрешното уво за губење на слухот предизвикано од бришење на везикуларниот транспортер на глутамат 3 (VGLUT3) генот;Посредувана од AAV1 испорака на егзогена VGLUT3 прекумерна експресија во клетките на влакното на внатрешното уво (IHCs) може да резултира со одржливо обновување на слухот, делумно обновување на синаптичката морфологија на лентата и конвулзивни одговори [4].Меѓутоа, во примерите вклучувајќи ги двете замени на генот испорачани со AAV опишани во воведот погоре, важно е да се забележи дека моделите на глувци што се користат за одредени типови на наследни нарушувања на губење на слухот со бришење на гени привремено се разликуваат од луѓето, а кај глувците P1, внатрешното уво е во зрела фаза на развој.Спротивно на тоа, луѓето се раѓаат со зрело внатрешно уво.Оваа разлика ја спречува можната примена на резултатите од глувчето за третман на човечки наследни нарушувања на глувоста, освен ако генската терапија не се доставува до уши на зрели глувци.
Уредување на гени: CRISPR/Cas9
Во споредба со „замената на гените“, развојот на технологијата за уредување на гени го донесе почетокот на лекувањето на генетските болести од корен.Поважно е тоа што методот на уредување на гени ги надополнува недостатоците на традиционалните методи на генска терапија со прекумерна експресија кои не се погодни за доминантни наследни болести на глувоста, како и проблемот што методот на прекумерна експресија не трае долго.Откако кинеските истражувачи конкретно го исфрлија мутантниот алел Myo6C442Y кај глувците Myo6WT/C442Y користејќи го системот за уредување на гени AAV-SaCas9-KKH-Myo6-g2, и во рок од 5 месеци од нокаутот, глувците Аудитивната функција на моделот беше вратена;во исто време, исто така беше забележано дека стапката на преживување на влакното во внатрешното уво е подобрена, обликот на цилиите стана правилен, а електрофизиолошките индикатори беа коригирани [5].Ова е прва студија во светот што ја користи технологијата CRISPR/Cas9 за третман на наследна глувост предизвикана од мутација на генот Myo6 и е важен истражувачки напредок на технологијата за уредување на гени за третман на наследна глувост.Клиничкиот превод на третманот обезбедува солидна научна основа.
Методи за испорака на генска терапија
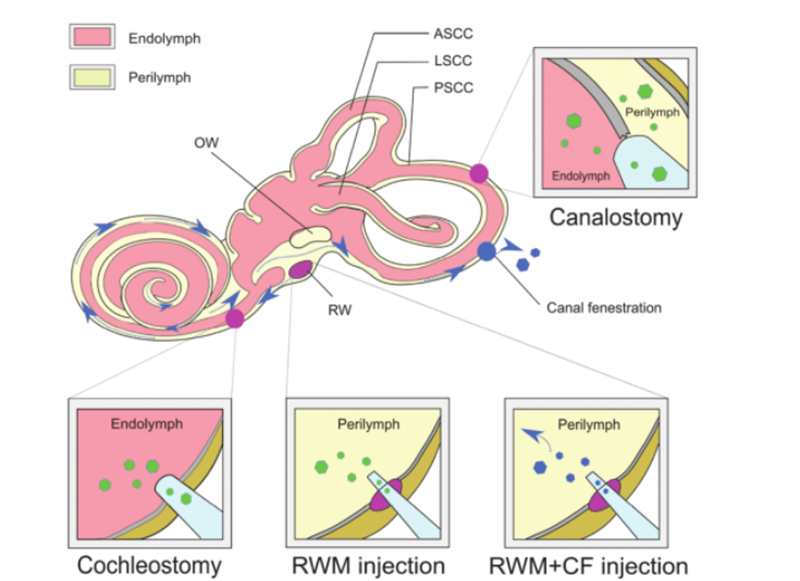
За да биде успешна генската терапија, голите молекули на ДНК не можат ефикасно да навлезат во клетките поради нивната хидрофилност и негативното полнење на фосфатните групи, а за да се обезбеди интегритет на дополнетите молекули на нуклеинска киселина, мора да се избере безбеден и ефикасен метод.Дополнетата ДНК се доставува до целната клетка или ткиво.AAV е широко користен како средство за испорака за третман на болести поради високиот инфективен ефект, ниската имуногеност и широкиот тропизам на различни типови ткива.Во моментов, голем број на истражувачки работи го утврдија тропизмот на различни подтипови на AAV во однос на различните типови на клетки во кохлеата на глувчето.Користењето на карактеристиките за испорака на AAV во комбинација со клеточно-специфични промотори може да постигне клеточно-специфична експресија, што може да ги намали ефектите надвор од целта.Дополнително, како алтернатива на традиционалните AAV вектори, постојано се развиваат нови синтетички AAV вектори и покажуваат супериорна трансдукциска способност во внатрешното уво, од кои AAV2/Anc80L65 е најшироко користен.Методите на не-вирусна испорака може дополнително да се поделат на физички методи (микроинјекција и електропорација) и хемиски методи (наночестички базирани на липиди, полимерни и златни наночестички).И двата пристапи се користени во третманот на наследни нарушувања на глувоста и покажаа различни предности и ограничувања.Во прилог на средството за испорака за генска терапија како средство, различни пристапи за ин виво администрација на гени може да се применат врз основа на различни типови целни клетки, начини на администрација и терапевтска ефикасност.Сложената структура на внатрешното уво го отежнува достигнувањето на целните клетки и дистрибуцијата на агенсите за уредување на геномот е бавна.Мембранозниот лавиринт се наоѓа во коскениот лавиринт на темпоралната коска и вклучува кохлеарен канал, полукружен канал, утрикула и балон.Неговата релативна изолација, минималната лимфна циркулација и одвојувањето од крвта со бариера од крвен лавиринт ја ограничуваат ефективната системска испорака на терапевтски средства само на неонатални глувци.За да се добијат вирусни титри погодни за генска терапија, неопходно е директно локално вбризгување на вирусни вектори во внатрешното уво.Воспоставените начини на инјектирање вклучуваат [6]: (1) кружна прозорска мембрана (RWM), (2) трахеостома, (3) ендолимфатична или перилимфатична кохлеостома, (4) мембрана на кружен прозорец плус фенестрација на цевка (CF) (како на Сл. 3).
Сл.3.Внатрешно уво испорака на генска терапија.
Иако е постигнат многу напредок во генската терапија, врз основа на клиничките преведувачки цели, треба да се направи повеќе работа пред генската терапија да стане опција за третман од прва линија за пациентите со генетски болести, особено во развојот на безбедни и ефективни вектори и метод на испорака.Но, ние веруваме дека во блиска иднина, овие типови третмани ќе станат главен производ на персонализирана терапија и ќе имаат огромно позитивно влијание врз животот на луѓето со генетски нарушувања и нивните семејства.
Foregene, исто така, лансираше комплет за скрининг со висока пропусност за насочени гени, кој е брз и може да изврши обратна транскрипција и qPCR реакции без екстракција на РНК.
Линкови за производи
Комплет Cell Direct RT-qPCR — Taqman/SYBR GREEN I
За повеќе информации за производот, ве молиме контактирајте:
Време на објавување: Сеп-02-2022 година